Η φαρμακευτική αγωγή του σακχαρώδη διαβήτη τύπου 2 πρέπει πάντα να προσαρμόζεται ξεχωριστά πάνω στον κάθε ασθενή. Εκτός από κάποιες γενικές κατευθυντήριες γραμμές, δίνεται μεγάλη ελευθερία στον γιατρό και τον ασθενή να αποφασίσουν από κοινού ποια θεραπεία ταιριάζει καλύτερα στο κάθε άτομο.
Ο αλγόριθμος που ακολουθείται παγκοσμίως είναι αυτός που συνοψίζεται στην παρακάτω εικόνα και προέρχεται από την Αμερικάνικη Διαβητολογική Εταιρία (American Diabetes Assosiation, ADA).
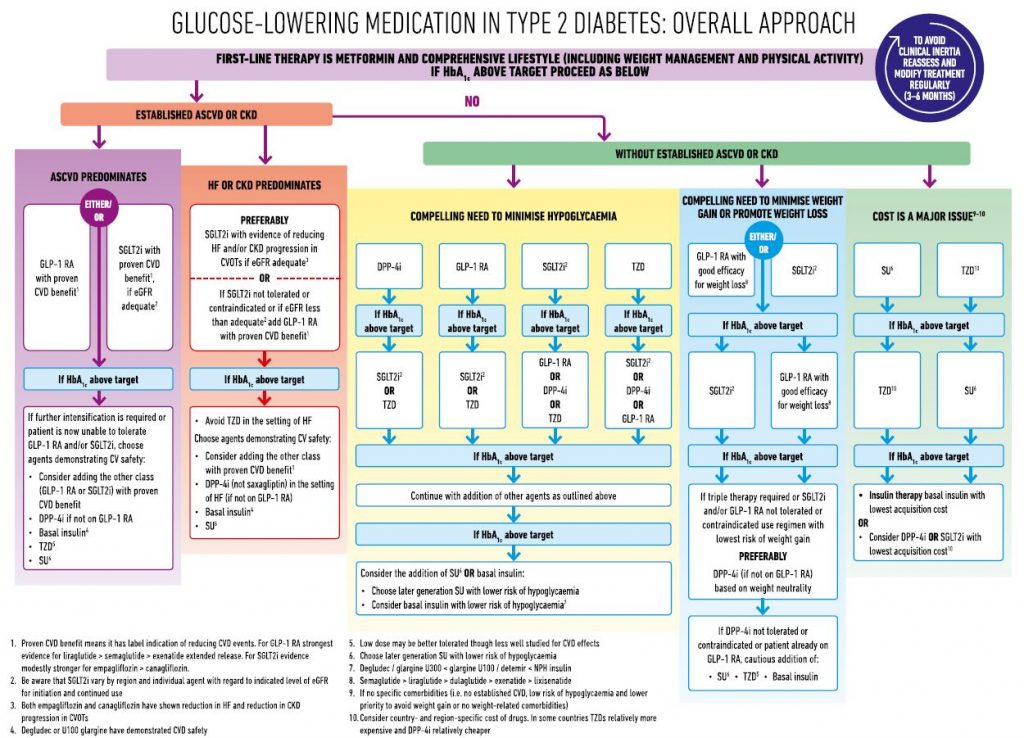
Ας δούμε κάθε μία από τις κατηγορίες φαρμάκων που εμφανίζονται στον παραπάνω πίνακα.
Διγουανίδια
Η μόνη ουσία της κατηγορίας που χρησιμοποιείται είναι η μετφορμίνη. Η μετφορμίνη είναι από τα παλαιότερα φάρμακα για το διαβήτη, αλλά ο ρόλος της παραμένει πολύ σημαντικός. Όπως φαίνεται και από τον παραπάνω αλγόριθμο, η μετφορμίνη είναι παρούσα σε κάθε θεραπευτικό βήμα. Είναι το πρώτο φάρμακο εκλογής, αλλά υπάρχει πάντα ως κομμάτι της θεραπείας και στους συνδυασμούς με άλλες ουσίες, ακόμα και με την ινσουλίνη.
Η μετφορμίνη μειώνει την παραγωγή σακχάρου από το ήπαρ, μειώνει την απορρόφηση της γλυκόζης από το έντερο και βελτιώνει την αντίσταση στην ινσουλίνη, βοηθώντας το σώμα να χρησιμοποιήσει καλύτερα τη γλυκόζη που λαμβάνει. Με αυτούς τους μηχανισμούς, η μετφορμίνη μειώνει και το σάκχαρο νηστείας, αλλά και το μεταγευματικό σάκχαρο.
Σε αντίθεση με άλλες κατηγορίες, προκαλεί πολύ σπάνια υπογλυκαιμίες, δηλαδή χαμηλό σάκχαρο. Επίσης, δεν επηρεάζει ιδιαίτερα το βάρος του ασθενούς, μπορεί μάλιστα να παρατηρηθεί μικρή μείωση. Οι κυριότερες παρενέργειές της είναι από το γαστρεντερικό (διάρροιες, κοιλιακά άλγη), που όμως δεν εμφανίζονται συχνά και είναι δοσοεξαρτώμενες. Η πιο επικίνδυνη παρενέργεια της μετφορμίνης είναι η γαλακτική οξέωση, που όμως είναι ιδιαίτερα σπάνια.
Γενικά, είναι ένα πολύ αποτελεσματικό, ασφαλές και οικονομικό φάρμακο, με ξεχωριστό ρόλο στη θεραπεία του διαβήτη τύπου 2.
Σουλφονυλουρίες
Οι σουλφονυλουρίες ήταν για χρόνια η δεύτερη δημοφιλέστερη κατηγορία θεραπευτικών ουσιών για τον διαβήτη, λόγω της αποτελεσματικότητάς τους και το μικρό τους κόστος. Καθώς όμως, ανεβάζουν κατά πολύ τον κίνδυνο υπογλυκαιμιών, που οδηγεί σχεδόν καθημερινά, κυρίως ηλικιωμένα άτομα που παίρνουν αυτά τα φάρμακα, σε νοσηλεία λόγω υπογλυκαιμιών, σταδιακά αυτή η κατηγορία έχει εγκαταλειφθεί, με κάποιες ίσως εξαιρέσεις, που θα αναφερθούν σε λίγο.
Ο μηχανισμός δράσης τους είναι μέσω της αυξημένης έκκρισης ινσουλίνης από το πάγκρεας και ίσως μέσω της ευαισθητοποίησης των διαφόρων ιστών στην ινσουλίνη. Το αποτέλεσμά τους είναι άμεσο, αλλά με το χρόνο φθίνει, καθώς το πάγκρεας εξαντλείται και δεν έχει δυνατότητα να παράγει παραπάνω ινσουλίνη. Επίσης, υπάρχει ένας μικρός κίνδυνος να προκαλέσουν αύξηση βάρους.
Οι δύο ουσίες της κατηγορίας που χρησιμοποιούνται ακόμα είναι η γλικλαζίδη και η γλιμεπιρίδη, πρέπει όμως πάντα να υπάρχει αυξημένος βαθμός εγρήγορσης για την παρουσία υπογλυκαιμιών.
Μεγλιτινίδες
Είναι ουσίες με παρεμφερή δράση με τις σουλφονυλουρίες, με το πλεονέκτημα ότι έχουν πολύ πιο σύντομη δράση, επομένως όταν δίνονται μαζί με το φαγητό, ο κίνδυνος υπογλυκαιμίας είναι μικρότερος. Είναι κι αυτές πολύ αποτελεσματικές, σε κοντινό βαθμό με τις σουλφονυλουρίες. Έχουν κι αυτές τον ίδιο κίνδυνο με τις σουλφονυλουρίες για αύξηση βάρους. Ένα άλλο πλεονέκτημά τους, είναι ότι μπορούν να δοθούν ακόμα και σε πολύ χαμηλή νεφρική λειτουργία.
Οι δύο χρησιμοποιούμενες ουσίες της κατηγορίας είναι η ρεπαγλινίδη και η νατεγλινίδη.
Θειαζολιδινεδιόνες
Οι ουσίες αυτές δρουν ευαισθητοποιώντας τον οργανισμό στην ινσουλίνη, επομένως χρειάζεται το πάγκρεας να έχει διατηρήσει κάποιο βαθμό λειτουργικότητας και να παράγει ινσουλίνη. Χρειάζεται θεραπεία για 12-16 εβδομάδες για να επιτευχθεί το μέγιστο αποτέλεσμα. Είναι οι μόνες ουσίες που έχουν δείξει να επιβραδύνουν την πρόοδο του διαβήτη, τουλάχιστον στα αρχικά στάδια.
Οι παρενέργειές τους είναι κυρίως η κατακράτηση υγρών και τα οιδήματα, καθώς και η αύξηση του βάρους. Ο κίνδυνος για υπογλυκαιμίες είναι πολύ μικρός, όπως και με τη μετφορμίνη.
Οι ουσίες που χρησιμοποιούνται είναι η πιογλιταζόνη και η ροζιγλιταζόνη. Η χρήση της δεύτερης είναι περιορισμένη, λόγω εμφάνισης υψηλότερου κινδύνου για καρδιακό έμφραγμα.
Αναστολείς DPP-4
Τα φάρμακα αυτής της κατηγορίας παρατείνουν τη δράση μιας ομάδας ορμονών που λέγονται ινκρετίνες. Οι ορμόνες αυτές μειώνουν το σάκχαρο στο αίμα διεγείροντας την έκκριση ινσουλίνης από το πάγκρεας μετά το φαγητό, καθυστερώντας την απορρόφηση της γλυκόζης από τον εντερικό σωλήνα και μειώνοντας το γλυκαγόνο, μια ορμόνη που αυξάνει το σάκχαρο. Επίσης, οι ινκρετίνες βοηθούν στο να δημιουργηθεί γρηγορότερα αίσθημα κορεσμού με το φαγητό.
Το DPP-4 είναι ένα ένζυμο που διασπά τις ινκρετίνες, κυρίως την GIP και το GLP-1. Επομένως, όταν αυτά τα φάρμακα εμποδίζουν το DPP-4, εμμέσως αυξάνεται η συγκέντρωση των ινκρετινών και η δράση τους.
Οι ουσίες που χρησιμοποιούνται είναι πέντε: λιναγλιπτίνη, σαξαγλιπτίνη, βιλνταγλιπτίνη, αλογλιπτίνη και σιταγλιπτίνη. Οι ουσίες αυτές μπορούν να χρησιμοποιηθούν είτε μόνες τους είτε σε συνδυασμό με άλλες κατηγορίες φαρμάκων. Είναι πολύ καλά ανεκτές από πλευράς παρενεργειών. Η λιναγλιπτίνη που μεταβολίζεται από το ήπαρ και όχι μέσω των νεφρών, μπορεί να δωθεί και σε χαμηλή νεφρική λειτουργία. Πολύ σπάνια προκαλούν υπογλυκαιμίες και δεν επηρεάζουν το βάρος των ασθενών. Ως νεότερη κατηγορία φαρμάκων είναι πιο ακριβή από τις προηγούμενες.
Αναστολείς SGLT-2
Αυτή είναι η νεότερη κατηγορία φαρμάκων από το στόμα για το διαβήτη. Αυτές οι ουσίες έχουν έναν ξεχωριστό μηχανισμό δράσης, επιτρέποντας στα νεφρά να αποβάλλουν μεγαλύτερες ποσότητες γλυκόζης στα ούρα. Έτσι, η παραπάνω γλυκόζη που κυκλοφορεί στο αίμα δε συσσωρεύεται και αποβάλλεται.
Λόγω του μηχανισμού δράσης, ο κίνδυνος για υπογλυκαιμίες είναι πολύ μικρός, αφού δεν επηρεάζεται η παραγωγή ινσουλίνης από το πάγκρεας. Ένα άλλο μεγάλο πλεονέκτημα αυτής της κατηγορίας είναι ότι προκαλεί απώλεια βάρους και μάλιστα σπλαχνικού λίπους. Δηλαδή, η απώλεια είναι πολύ ωφέλιμη για το σώμα. Τα φάρμακα αυτά έχουν κάποια διουρητική δράση και μπορεί να παρατηρηθεί μείωση της αρτηριακής πίεσης.
Ως παρενέργεια, παρατηρήθηκε μια σχετικά μικρή αύξηση των ουρολοιμώξεων, που όμως δεν προκαλούσαν ιδιαίτερα προβλήματα στους ασθενείς.
Οι ουσίες που κυκλοφορούν στην Ελλάδα είναι δύο, η εμπαφλιγλοζίνη και η νταπαφλιγλοζίνη και η καναγλιφλοζίνη. Νεότερες έρευνες που δημοσιεύθηκαν μέσα στο 2016 για την εμπαφλιγλοζίνη δείχνουν ότι με τη χρήση αυτής της ουσίας μειώνεται ο κίνδυνο για καρδιαγγειακά νοσήματα στους ασθενείς με διαβήτη και προφυλάσσεται η νεφρική λειτουργία.
Ενέσιμα φάρμακα
Αγωνιστές υποδοχέων GLP-1
Αυτή η κατηγορία φαρμάκων επιδρά στο σύστημα των ινκρετινών, όπως και οι αναστολείς του DPP-4. Το πλεονέκτημά τους είναι ότι δεν εξαρτώνται από την ενδογενή παραγωγή ινκρετινών για να δράσουν. Έχουν δράση παρόμοια με τις ινκρετίνες του σώματος και αυξάνουν την έκκριση ινσουλίνης αλλά με τρόπο γλυκοζοεξαρτώμενο, δηλαδή όταν αυξάνει η γλυκόζη αυξάνει και η ινσουλίνη και όχι γενικά, όπως γίνεται με τις σουλφονυλουρίες.
Είναι πολύ αποτελεσματικά φάρμακα, περισσότερο από τους αναστολείς DPP-4, έχουν κι αυτά πολύ μικρό κίνδυνο για υπογλυκαιμίες και έχουν θετική επίδραση στο βάρος, δηλαδή οι ασθενείς χάνουν σχεδόν πάντα κάποια κιλά.
Έχουν συνήθως κάποιες παρενέργειες από το γαστρεντερικό σύστημα, όπως έντονη τάση προς έμετο, που όμως φεύγουν με τον καιρό.
Επειδή είναι σε ενέσιμη μορφή συχνά συγχέονται με τις ινσουλίνες, όμως είναι ένα εντελώς διαφορετικό φάρμακο. Οι κύριες ουσίες που εκπροσωπούν την κατηγορία είναι η λιραγλουτίδη, η ντουλαγλουτίδη και η σεμαγλουτίδη. Η λιραγλουτίδη είναι η πρώτη χρονικά ουσία που κυκλοφόρησε στην κατηγορία. Οι ντουλαγλουτίδη και σεμαγλουτίδη είναι σε εβδομαδιαία μορφή. Και οι 3 αυτές ουσίες έχει παρατηρηθεί ότι προκαλούν σημαντική απώλεια βάρους. Μάλιστα, η λιραγλουτίδη κυκλοφορεί με δύο εμπορικές ονομασίες, μία με ένδειξη τον διαβήτη τύπου 2 και μία, ελέυθερη συνταγής, με ένδειξή την παχυσαρκία, όπου απευθύνεται σε μη διαβητικούς ανθρώπους.
Ινσουλίνες
Λόγω της φυσικής πορείας της νόσου του διαβήτη, όλοι οι ασθενείς κάποια στιγμή αναπτύσσουν έλλειμα ινσουλίνης. Ο μόνος τρόπος να διορθωθεί αυτό το έλλειμα, όσο καλή κι αν είναι η θεραπεία με φάρμακα από το στόμα, είναι μέσω της ινσουλίνης.
Η ινσουλίνη είναι η ορμόνη εκείνη που φυσιολογικά εκκρίνεται από τα β-κύτταρα του παγκρέατος και βοηθάει κάθε κύτταρο του οργανισμού να προσλάβει και να χρησιμοποιήσει ως ενέργεια τη γλυκόζη. Επειδή είναι μία ουσία που φυσιολογικά υπάρχει στο σώμα, η θεραπεία με ινσουλίνη δεν έχει άλλες παρενέργειες εκτός της υπογλυκαιμίας και της αύξησης του βάρους στην αρχή της θεραπείας. Η ινσουλίνη μπορεί να δοθεί σε οποιοδήποτε επίπεδο νεφρικής λειτουργίας, ακόμα και σε ασθενείς σε αιμοκάθαρση.
Είναι το πιο αποτελεσματικό φάρμακο για το διαβήτη. Νεότερες τάσεις είναι υπέρ του να μπαίνει η ινσουλίνη σε αρκετά πρώιμο στάδιο στο διαβήτη, γιατί έτσι προστατεύεται το πάγκρεας και μπορεί να λειτουργεί για πολλά περισσότερα χρόνια. Παραδοσιακά, η θεραπεία με ινσουλίνη στη χώρα μας τείνει να φοβίζει τους ασθενείς. Ο φόβος αυτός όμως, ίσως να μπορεί να μειωθεί, αν ο ασθενής συζητήσει για τη θεραπεία αυτή με το γιατρό του και λάβει αρκετές πληροφορίες ώστε να δει ότι η θεραπεία με ινσουλίνη αφενός έχει εκσυγχρονιστεί σε σχέση με παλαιότερα χρόνια και αφετέρου είναι αναμφίβολα η πιο αποτελεσματική για την πτώση των επιπέδων της γλυκόζης.
Φυσιολογικά, το πάγκρεας παράγει μια μικρή ποσότητα ινσουλίνης συνεχόμενα, η οποία διατηρεί τη γλυκόζη σε ένα σταθερό επίπεδο. Στα γεύματα, λόγω της αύξησης του σακχάρου, υπάρχει η αντίστοιχη αύξηση της ινσουλίνης από το πάγκρεας. Στο παρακάτω γράφημα φαίνεται ακριβώς το πώς εκκρίνεται η ινσουλίνη μέσα σε ένα εικοσιτετράωρο από το πάγκρεας.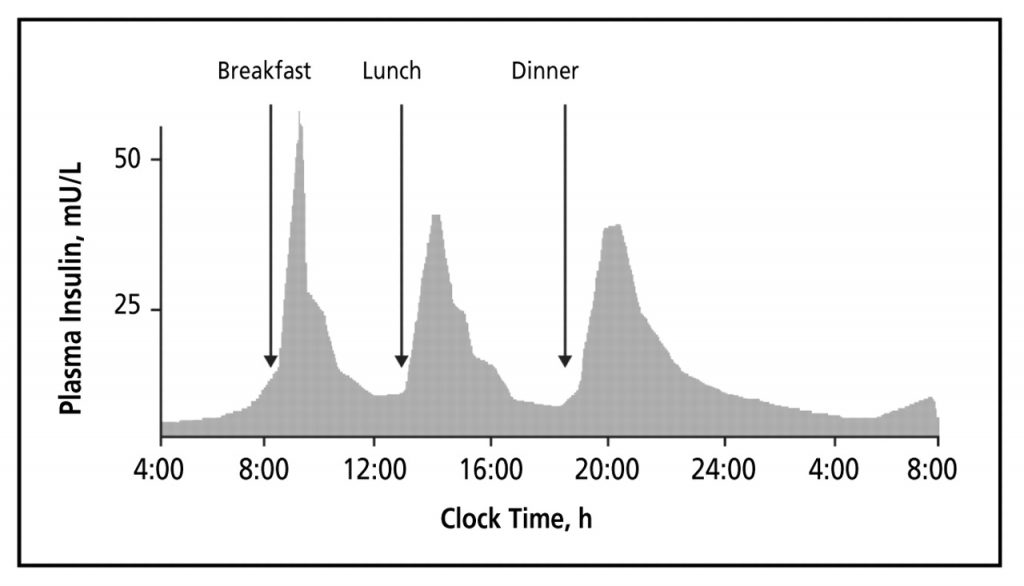
Αυτή τη φυσιολογική έκκριση προσπαθούμε να μιμηθούμε όταν δίνουμε ινσουλίνη με τη μορφή ημερήσιων ενέσεων.
Γενικά, οι διάφοροι τύποι ινσουλίνης που κυκλοφορούν μπορούν να χωριστούν σε δύο μεγάλες κατηγορίες, τις βασικές ινσουλίνες και τις ταχείας δράσης.
Οι βασικές ινσουλίνες που κυκλοφορούν είναι η συνθετική ανθρώπινη (Humulin NPH), η ινσουλίνη detemir (Levemir), η ινσουλίνη glargine (Lantus, Abasaglar) και η ινσουλίνη degludec (Tresiba). Διαφέρουν στον χρόνο δράσης, όπως φαίνεται στο παρακάτω γράφημα (όπου φαίνεται και η διαφορά με τις ινσουλίνες ταχείας δράσης):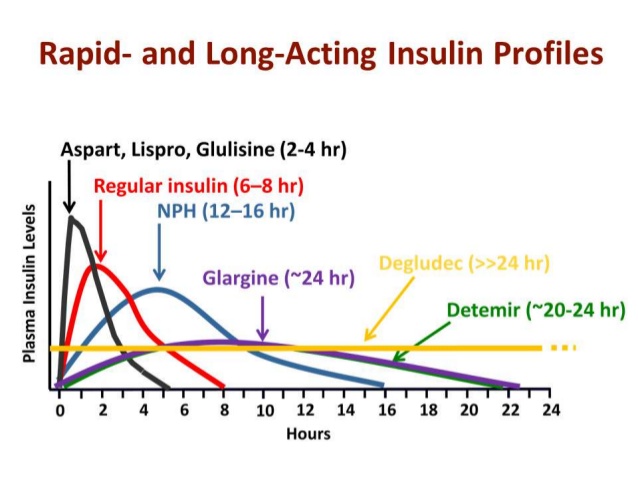
Οι ινσουλίνες ταχείας δράσης είναι οι εξής: ινσουλίνη lispro (Humalog), ινσουλίνη aspart (Novorapid), ινσουλίνη glulisine (Apidra) και η συνθετική ανθρώπινη ινσουλίνη ( Insuman, Humulin και Actrapid που είναι ενδιάμεσης δράσης).
Κυκλοφορούν και οι έτοιμοι συνδυασμοί βασικής και ταχείας δράσης, δηλαδή μείγματα όπου η ταχείας δράσης ινσουλίνη αποτελεί ένα ποσοστό από 25-50% του μείγματος και το υπόλοιπο αποτελείται από βασική ινσουλίνη.
Υπάρχουν πολλές διαφορετικές στρατηγικές στη χρησιμοποίηση των διαφόρων ινσουλινών, ανάλογα με τις ανάγκες του κάθε ασθενούς. Τα θεραπευτικά σχήματα μπορεί να ποικίλουν από μία ένεση βασικής ινσουλίνης ή μείγματος την ημέρα μέχρι τα εντατικά σχήματα με μία ή δύο ενέσεις βασικής το εικοσιτετράωρο σε συνδυασμό με τρεις ενέσεις ταχείας ινσουλίνης μαζί με τα γεύματα.
Κατά την έναρξη θεραπείας με ινσουλίνη πρέπει ο ασθενής να ενημερώνεται διεξοδικά για τις υπογλυκαιμίες, δηλαδή το χαμηλό σάκχαρο στο αίμα. Είναι σχεδόν σίγουρο ότι κάθε διαβητικός που λαμβάνει ινσουλίνη θα εμφανίσει κάποια στιγμή στη ζωή του υπογλυκαιμία. Τα κλασσικά συμπτώματα της υπογλυκαιμίας είναι τρόμος στα χέρια, έντονη εφίδρωση και θολή όραση. Οι υπογλυκαιμίες χωρίζονται σε σοβαρές και ήπιες. Σοβαρές είναι αυτές όπου ο ασθενής χρειάζεται βοήθεια από κάποιο άλλο άτομο για να ξεπεράσει την υπογλυκαιμία, ήπιες είναι εκείνες όπου ο ασθενής εγκαίρως προλαβαίνει να φάει ή να πιει κάτι ώστε να ανέβει το σάκχαρο και να υποχωρήσει η υπογλυκαιμία. Εκείνη τη στιγμή, καλό είναι να καταναλώνεται κάτι που θα ανεβάζει τη γλυκόζη άμεσα, όπως ένας κύβος ζάχαρης, ένα ποτήρι χυμός ή κάτι άλλο γλυκό.
Μια άλλη σημαντική διαφορά μετά την έναρξη της ινσουλίνης είναι ότι απαιτούνται πολλές μετρήσεις σακχάρου ημερησίως, καθώς οι μετρήσεις αυτές είναι το μόνο εργαλείο που έχουμε για να ρυθμίσουμε κατάλληλα την ινσουλίνη και να επιτύχουμε ιδανικό έλεγχο, καθώς και να αποφύγουμε τις υπογλυκαιμίες.
Μετά από συζήτηση του ασθενούς με το γιατρό μπορούμε να βρούμε το κατάλληλο σχήμα που να ταιριάζει σε κάθε ασθενή, ώστε να επιτυγχάνουμε τον καλύτερο δυνατό έλεγχο του διαβήτη, με όσο το δυνατόν λιγότερες, αν γίνεται και καθόλου, υπογλυκαιμίες.